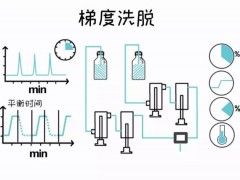
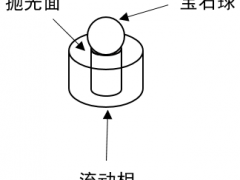
新药申报时,药品质量标准中分析方法必须验证;药物生产工艺变更、制剂的组分变更、原分析方法进行修订时,质量标准分析方法必须进行验证。
一、分析方法学验证事项
药物分析检验时药品生产的GMP的药物分析的方法学验证,是保证药物分析结果准确性的前提和基础,也是实现药物分析检测GMP的必然要素。构成药物分析中的检测方法验证,涉及以下方面的内容:
1、分析方法验证成功的前提条件:
(1)仪器已经确认、校正并在有效期内
(2)经过培训的人员
(3)可靠稳定的对照品
(4)可靠稳定的实验试剂
(5)确认受试溶液的稳定性,在规定时间内无降解
2、分析方法学验证所要求验证的内容:
(1)含量的测定
(2)杂质的含量测定
(3)药物的定性鉴定
(4)药物的含量均匀度测定
(5)药物的微生物检测
(6)药物的细菌内毒素的检测
图片
验证内容
图片
准确度:
准确度是指用该方法测定的结果与真实值或参考值接近的程度,用百分回收率表示。
测定回收率R(recovery)的具体方法可采用加样回收试验法来进行测定。加样回收试验已准确测定药物含量P的真实样品+已知量A的对照品(或标准品)测定,测定值为M。
数据要求:规定的范围内,至少用9次测定结果评价,如制备高、中、低三个不同浓度样品各测三次
精密度:
(重复性、中间精密度和重现性精密度是指在规定条件下,同一个均匀样品,经多次取样测定所得结果之间的接近程度。用偏差(d)、标准偏差(SD)、相对标准偏差(RSD)(变异系数,CV)表示。
(1)重复性(repeatability):在相同条件下,由同一个分析人员测定所得结果的精密度;在规定的范围内,至少用9次测定结果评价,如制备三个不同浓度样品各测三次或把被测物浓度当作100%,至少测6次进行评价
(2)中间精密度:同一实验室,不同时间由不同分析人员用不同设备所得结果的精密度
(3)重现性(reproducibility):不同实验室,不同分析人员测定结果的精密度
(4)数据要求:需报告SD,RSD和可信限
专属性:
指有其他成分(杂质、降解物、辅料等)可能存在情况下采用的方法能准确测定出被测物的特性,能反映该方法在有共存物时对供试物准确而专属的测定能力,是指该法用于复杂样品分析时是否受到相互干扰程度的度量
• 通常通过分析含有加了杂质、降解产物、有关化学物质或安慰剂成分的样品,将所获分析结果与未加前述成分之样品的测试结果进行比较,两组测试结果之差即专属性
•鉴别反应---应能与可能共存的物质或结构相似化合物区别,不含被分析的样品,以及结构相似或组分中的有关化合物,均应呈负反应
•含量测定和杂质测定---色谱法和其他方法,应附代表性图谱,亦说明专属性;图中应标明各组份的位置,色谱法中的分离度应符合要求
•杂质可获得的情况下,对于含量测定,试样中可加入杂质或辅料,考察测试结果是否受干扰;对于杂质测定,也可向试样中加入一定量的杂质,考察杂质间是否得到分离
检测限:
检测限系指试样在确定的实验条件下,被测物能被检测出的最低浓度或含量;它是限度检验效能指标,无需定量测定,只要指出高于或低于该规定浓度即可
•非仪器分析目视法:用已知浓度的被测物,试验出能被可靠地检测出的最低浓度或量
•信噪比法:用于能显示基线噪音的分析方法(仪器分析方法),是把已知低浓度试样测出的信号与空白样品测出的信号进行比较,算出能被可靠地检测出的最低浓度或量;一般以信噪比3∶1或2∶1时的相应浓度或注入仪器的量确定检测限
•也可采用标准差法:
空白值=0时;
①测定背景10次以上,求出标准差σ;
②将σ乘以三倍;
③在工作曲线上求出3σ相对应的浓度X,即为方法的检出值。
空白值不等于0时;
①测定背景10次以上,求出标准差σ;
②将σ乘以三倍;
③在工作曲线上求出3σ相对应的浓度X;
④将求得的对应浓度值加上空白值即得该方法的检出限。
图片
定量限(limit ofquantitation LOQ)
•指样品中被测物能被定量测定的最低量,结果应具有一定准确度和精密度要求
•常用信噪比法确定定量限,一般以信噪比(S/N)为10∶1时相应的浓度或注入仪器的量进行确定,也可用仪器所测空白背景响应标准差(SD)的10倍为估计值,再经试验确定方法的实际测定下限
线性:
在设计的范围内,测试结果与试样中被测物浓度直接呈正比关系的程度。线形通常用最小二乘法处理数据求得回归曲线的斜率(Slope)来表示。数据要求:至少需要五个浓度考察线形,需提供相关系数、y截距(是检定的可能偏差)、回归斜率及方差等参数,应列出回归方程数和线性图。
注意:做线性时,应注意尽量做的点多一点、线性浓度范围宽一点,这样做的好处是:当你在准确度考察时,你做的回收率考察的浓度就大些,配制溶液时就容易操作些;否则,在你做线性考察时,你做的线性浓度范围不宽,那么你在考察回收率时,你采用加入法考察时的浓度变化范围就不宽,操作浓度很难控制,造成实际操作困难。
范围:
指达到一定精密度、准确度和线性的条件下,测试方法适用的高、低限浓度或量的区间。范围应根据分析方法的具体应用和线性、准确度、精密度结果和要求确定。
•原料药和制剂含量测定范围为80%-120%;制剂含量均匀度范围为70%-130%;杂质测定应为被测杂质汇报值到限度的120%;溶出度应为测定范围的±20%,如规定了限度范围,应为下限的-20%至上限的+20%,例如缓释片1h<20%,7h>70%,则验证范围定为0-90%。
耐用性:
指测定条件稍有变动时,结果不受影响的承受程度,为常规检验提供依据。是衡量实验室和工作人员之间在正常情况下实验结果重现性的尺度;如果方法易受到分析条件的影响,或要求苛刻,应注明。
典型的变动包括:分析溶液的稳定性,提取时间等。
版权与免责声明:
① 凡本网注明"来源:科学仪器网"的所有作品,版权均属于科学仪器网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:科学仪器网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认科学仪器网有权转载。
 手机版|
手机版|

 二维码|
二维码|